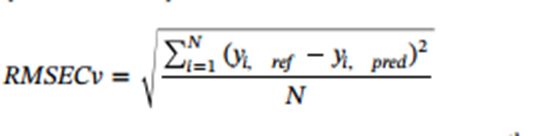生物上游过程工艺开发阶段通过拉曼光谱提高对mAb生产的可靠性
作者:艾贝泰 2023.09.04 点击259次
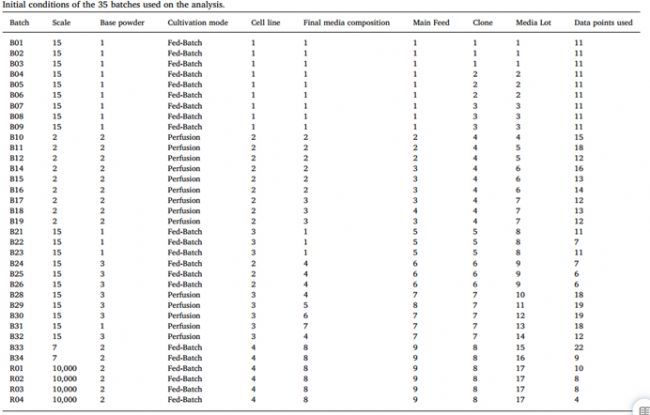
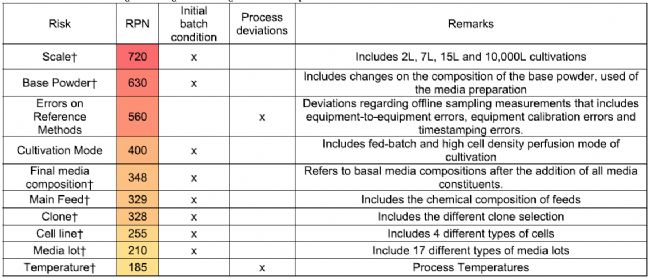
01背景拉曼技术在生物工艺开发中的应用已经显示出其在培养工艺和过程监测的巨大潜力。但在生物工艺开发过程中,当克隆、培养基或培养规模等条件发生变化时,拉曼技术的性能仍面临一些挑战和限制。本研究提出了一种实用的PAT(过程分析技术)监测方法,既可用于开发阶段,也可用于生产阶段,以平衡生物工艺开发过程中多个哺乳动物细胞培养过程中产生的不同结果。将风险评估技术与开发监测定标(局部模型或一般模型)的两种方法相结合,当多种培养条件发生变化时,我们能够从作为PAT工具的拉曼光谱中获得良好的预测能力。本篇文章使用四种不同类型的CHO细胞、八种不同的克隆和四种不同的规模(2升、7升、15升和10000升),在两种培养模式(分批培养和灌流培养)下进行了35次培养,在生物工艺开发的同时使用拉曼在线生物工艺分析仪最好地开发PAT方法提供参考。 02介绍过程分析技术(PAT)于2004年由美国食品药品管理局(FDA)发起。新一代基于过程分析技术的制药研发和生产程序允许从中间体和最终产品的抽样检测质量转向基于对材料属性、过程参数和产品质量属性之间关系的正确理解的设计质量(QbD)。PAT在生物制药领域的发展缓慢而稳定主要有以下几个原因:缺乏具有必要灵敏度和特异性的PAT工具来区分主产品和多种副产品;由于基于细胞的过程会产生多组分基质,光谱选择性降低;在标称培养条件下,不同时间和不同属性之间的自相关性较高。由于拉曼技术具有采集速度快、无创伤、无试剂、精确度高和单个样品成本低等特点,因此在监测生物过程(特别是上游过程)方面备受关注。与需要人工取样的传统参考分析方法相比,原位在线拉曼光谱具有多种优势。拉曼光谱是一种非常强大的PAT工具,在适当校准的情况下,可提供近乎实时的过程状态估计。在过去十年中,许多研究将拉曼光谱定位为生物制药加工过程(即以卵巢细胞(CHO)为平台的单克隆抗体(mAb))的适用PAT工具。其中一些研究侧重于拉曼光谱和反馈控制策略,另一些研究则证明了拉曼光谱在监控从研发到生产的不同培养条件和规模方面的可行性。近期研究表明,使用选择方法并将拉曼光谱区域分配给特定的分析物,同时进行成分加标研究,可以提高模型的预测能力。 本研究旨在为在工艺开发阶段评估影响校准模型开发的主要因素奠定基础。它还有助于引入最佳实践,将可靠性纳入PAT监测方法,使其成为离线参考分析方法的可行替代方法。最终目的是通过使用PAT方法及其工艺监测强化,缩短开培养时间,同时从产品发布开始就提供稳健的工艺。因此,我们将研究不同工艺参数和培养条件对拉曼光谱模型性能的影响。我们建议采用基于风险优先级数(RPN)的风险策略,对影响拉曼光谱性能的不同变化源进行排序和选择。选定的变化源,即批次条件,也将通过使用多变量统计过程监控来测试其对拉曼光谱数据的影响。针对葡萄糖、乳酸盐和蛋白质浓度这三种关键分析物,在每一批次条件下比较非特定通用模型和小型特定模型生成的模型统计参数,然后进行评估。 03材料和方法3.1 实验配置 本研究采用4种不同类型的CHO细胞系、8个不同的克隆、4种不同的规模(2L、7L、15L和10000L),在标称操作条件(NOC)下分批补料和灌注两种培养模式进行35次培养。表1总结了可用的批次,参考了它们各自的条件(探索了八种不同的批次条件或因素)。这些用于标记每个批次的光谱数据。 较小的生物反应器(最多15升)是玻璃容器(Applikon Biotechnology,荷兰),而生产10000升的生物反应器是不锈钢容器。所有仪器都配备了pH值、温度、溶解氧探针和拉曼探针。使用Kaiser Raman Rxn2 (Kaiser Optical Systems, USA)仪器。拉曼系统配备785 nm激发激光系统和四个浸没探针,长度分别为120mm(10000L容器),220mm(2L容器)和420mm(7和15L容器)。光谱采集范围为400-1800cm−1,扫描75次,每次扫描10s。大约每天从每个反应器中抽取一次样本进行参考分析。葡萄糖和乳酸使用NOVA Biomedical (Massachusetts, USA)的BioProfile FLEX进行分析。蛋白质浓度采用高效液相色谱专有定量方法进行分析。 3.2 风险评估 本研究中的风险评估由分析方法开发和哺乳动物细胞生物工艺开发方面的多学科专家团队进行。专家们根据严重性(S)、发生率(O)和可检测性(D)对风险进行了评估,并将获得最佳条件(高蛋白浓度、产量和高存活细胞密度)这一目标的风险作为评估的问题陈述。在评估过程中,根据这些因素的乘积RPN对每种条件进行排序。然后,通过标准的故障模式和影响分析法(FMEA)完成风险评估工作。潜在因素分为两类,一类取决于批次条件,另一类则不取决于批次条件。取决于批次变化的风险因素被称为不可控因素,可能带来随机或系统误差(如与离线测量相关的误差)。风险评分与批次演变无关的因素,即初始批次条件,可在培养前通过选择适当的受控批次条件来降低。对于RPN值低于200且与批次变化无关的风险,则不予考虑。 3.3 数据分析 在三十五个批次中获取的所有光谱均被导入Matlab8.5 2015(MathWorks,Natick,MA,USA)。每个批次由经过光谱预处理的12个点的平均值组成:第1次导数(25点窗口),然后是标准正态变异(SNV)。在批次级分析中,所有收集到的光谱都按时间顺序排列,以创建批次进化模型(BEM)。通过主成分分析法(PCA),利用该模型的得分建立批次水平模型(BLM)。在BLM的得分图中,每个点代表三十五个批次中的一个,它们在图中的位置由光谱变异性决定。在本地模型分析中,光谱数据分类的较小单位是批次。具有相同特征的批次组(例如,所有2L批次)以等级表示。与某类批次特征(如刻度)相关的级别组被称为批次条件。批次条件之间的关系相同的,则视为处于连续的阶段(例如,每个细胞系(阶段1)可衍生为不同的克隆(阶段2))。数据使用偏最小回归法(PLS)建立模型,其中拉曼位移为自变量(X变量),离线代谢物和蛋白质浓度测定为因变量(Y变量)。模型的整体性能以均方根e。
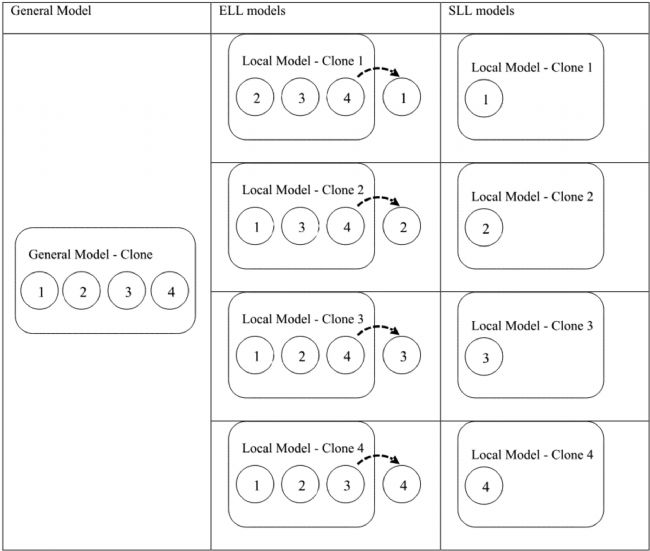
模型建立过程包括利用35个批次的所有可用光谱数据创建PLS模型(通用模型),同时利用特定级别(一个或多个不同批次)的不同光谱数据集创建较小的PLS模型(局部模型)。创建局部模型采用了两种策略。第一种策略是在批次条件的指导下建立本地模型。对于每个模型,校准集由在特定条件下收集的所有光谱构成,但校准集中不包括特定级别的光谱。这种"只留一级"的策略被称为"排除级局部建模(ELL)"。因此,对于每个批次条件,我们将根据每个批次条件中的等级数量来建立相同数量的 ELL 模型。第二种策略是只使用与单个级别相对应的光谱来建立局部模型。我们称这种策略为单级局部(SLL)建模。对于每个批次条件,我们的SLL模型数量与每个批次条件中的等级数量相同。图1以批次条件"克隆"为例说明了上述校准策略。
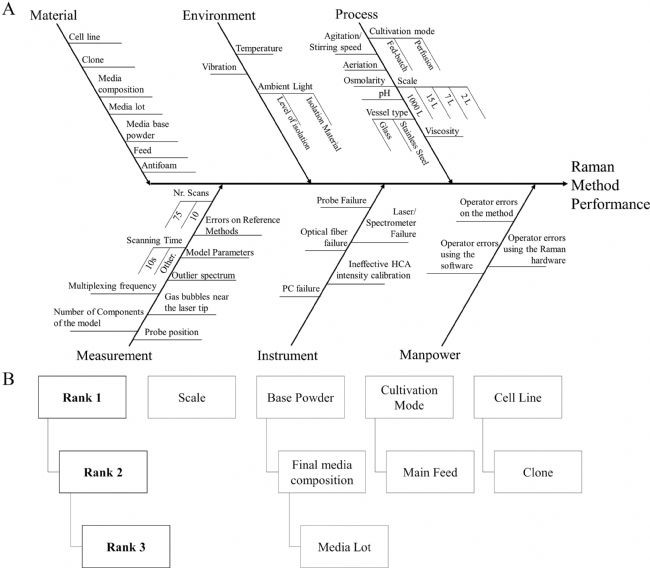
04结果4.1 初步风险评估 使用鱼骨图或石川图图2-A列出并整理所有风险,进行初步风险评估。风险按照材料、环境、工艺、测量、仪器和人力进行分类。图2-B显示了本研究分析的批次条件之间的层次和依赖关系。具有相同养育关系的批次条件共享同一阶段。对风险进行FMEA分析,筛选出与批次演变相关的风险。 通过确定最小 RPN 值为 200,我们可以将重点放在8个可能事先影响拉曼信号的潜在风险的影响上(表1)。
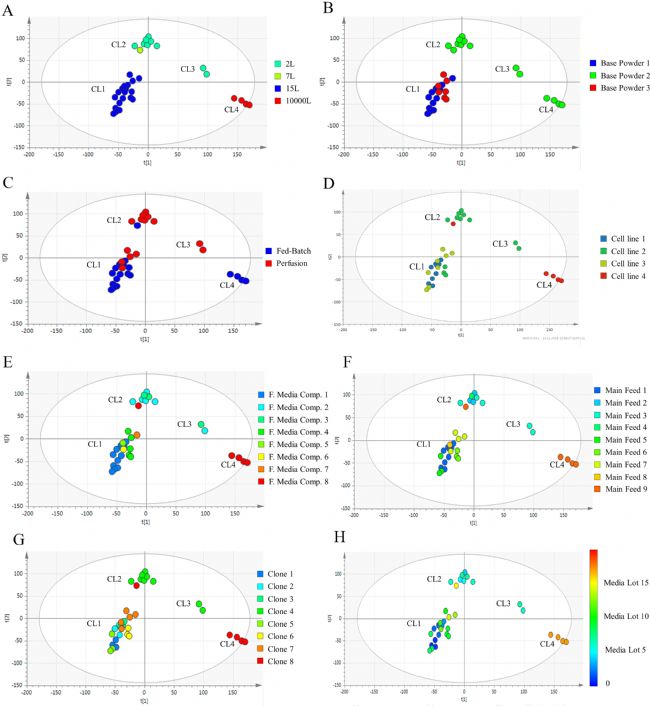
图3显示了批次级PCA前两个主成分的得分。相同的得分图以倍数表示(A至H),并根据不同的批次条件使用不同的色标。35个批次的得分图呈现出四个主要群组(CL1至CL4)。当按比例对评分图着色时(图3-A),CL1组对应15升批次(深蓝色);CL2组对应2升批次(浅蓝色)和单个7升批次(浅绿色);CL3组对应2升批次(浅蓝色);CL4组对应10000升批次(红色)。当按培养基对得分图着色时(图3-B),群组CL1同时对应培养基1(深蓝色)和培养基3(红色);培养基2(浅绿色)在该图的其余群组上被识别。在其余批次条件下,同样的聚类识别并不清晰。当按培养模式对得分图着色时(图3-C),CL3和CL4组分别对应于灌流和分批培养,而CL1和CL2组则显示出两种培养模式的混合。按细胞系(图3-D)、最终培养基成分(图3-E)、主要进料(图3-F)、克隆(图3-G)和培养基批次(图3-H)着色时也呈现出同样的趋势,其中CL1和CL2显示出多个不同级别的批次。
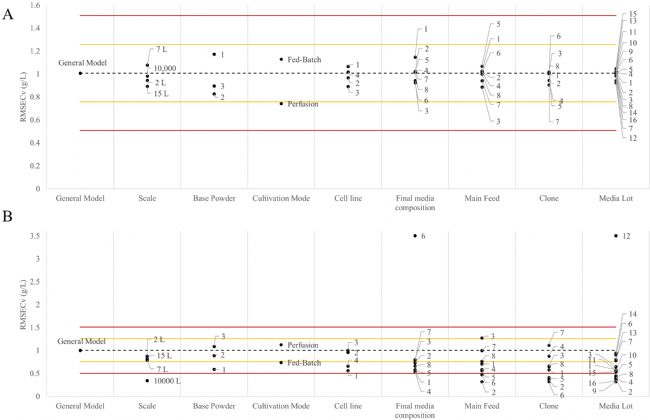
4.2 本地模型分析 为了比较每个批次条件下各层次生成的所有局部模型,本研究采用了一种类似于控制图的可视化方法,其中x轴对应于每个批次条件。所有散点表示每个局部模型在各自批次条件下的RMSECv。中心虚线用作基线,表示使用每种分析物的所有可用数据计算的通用模型RMSECv值(通用 RMSECv)。虚线上下的黄线分别表示一般模型RMSECv的±25%。上下红线的作用相同,表示一般模型RMSECv的±50%。在ELL模型中,RMSECv 值与一般RMSECv的变化量不同于SLL模型。如果ELL和SLL模型的RMSECv值低于一般模型的该参数,则该分析将认为ELL和SLL模型是可接受的。换句话说,所有批次条件都要求其所有局部模型的RMSECv值低于每个一般模型的0%。 图4是葡萄糖的ELL模型和SLL模型
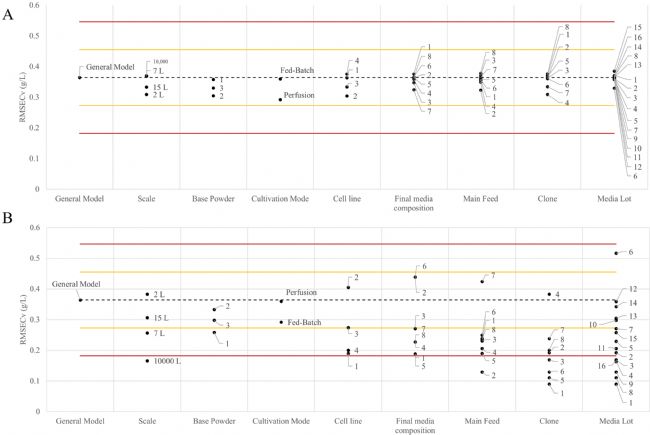
图5是乳酸浓度的ELL模型和SLL模型
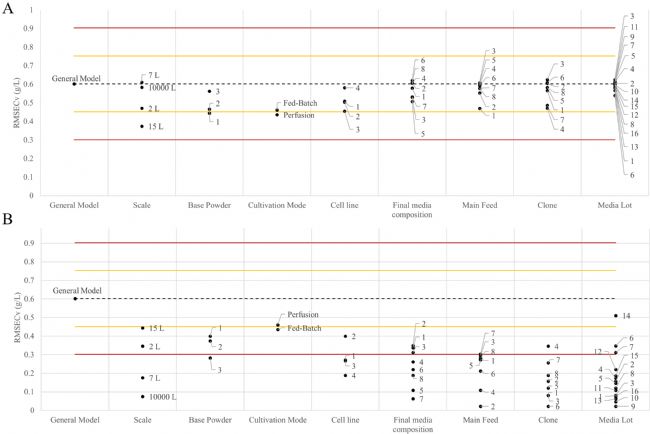
图6是蛋白质浓度的ELL模型和SLL模型
表2总结了针对8个批条件建立的局部模型的结果,包括批级PCA、级别模型和随着获得更多的过程相关知识,可以通过重复风险评估来重新评估现有的过程理解。使用批级PCA聚类分析、ELL和SLL建模、使用批次范围和本地模型数量的每批条件输出摘要。标记为黄色的RMSECv百分比表示所有本地模型在+25%和-50%的区间内,绿色表示所有本地模型低于0%的批量条件。在至少一个本地型号高于±50%的批量条件下,用红色标记的RMSECv百分比。
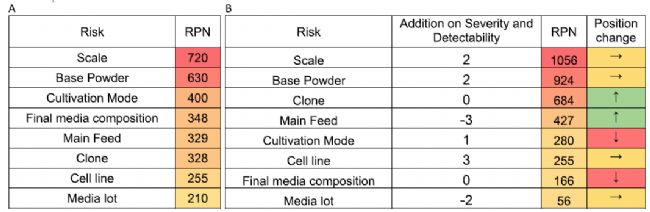
因此,表3中的初始风险评估可以使用批级PCA、ELL、SLL和用于局部模型的批次数的结果进行更新(表4)。初始风险分析(A)和最终风险分析(B),基于批级PCA、ELL和SLL的结果,考虑了每个批条件的影响。
05讨论RMSECv是一个比预测均方根误差(RMSEP)-外部预测更好的指标。这是因为不同的局部模型与外部预测之间的比较需要对两个局部模型进行相同级别的验证批次处理。最佳RMSEP偏向于与验证批次共享相同级别的局部模型。为每个局部模型使用定制的外部验证批次不仅需要额外使用设备,而且还需要编译所有RMSEP值,以便建立适当的比较。使用模型的不同配置,以结构的方式,并编译所有不同的RMSEP值是RMSECv的最终目标,这使其成为本研究中最合适的方式。 PAT方法的使用在工艺开发期间尤为重要。使用来自多个生物反应器规模(即水平规模)的数据需要使用特定于每个生物反应器规模的本地模型,无论是使用SLL还是ELL模型,按比例进行模型分类产生了可行的结果(见表3),其中RMSECV不高于一般模型的10%。将这个方法用于葡萄糖和乳酸,并将这一结论扩展到蛋白质浓度。一方面,单比例模型可以简化规模放大,使用低成本的小批量作为校准来验证大批量。 对于培养模式来说,分批培养和灌流培养ELL和SLL建模都有互补的校准集。这种批次条件产生的局部模型在ELL和SLL建模中范围最广,其中一些模型RMSECv高于通用模型的RMSECv。批次条件下的细胞系在使用SLL或ELL时,在相同范围内的局部模型都有较好的结果。 综上所述,该研究证明与通用模型相比,使用以批量条件为导向的模型构建策略,所有局部模型的预测误差都会减小。使用少量批次(3-9个)就能生成预测误差较低的局部模型,这可以作为生产阶段的校准策略。批次条件也显示使用类似的批次数量范围(1-9),可产生较低的RMSECv值,是克隆的较好替代方案。 研究表明,评估影响拉曼光谱校准模型的因素是提高该监测预测性能的关键。在工艺开发过程中,拉曼监测模型提供准确和精确的预测,在许多工艺参数组合发生变化时同样可以精准预测。比较通用模型的RMSECv和特定本地模型的RMSECv,用于每个批次条件下的单个过程特征。通过构建这些局部模型的方法,比较了通用模型(ELL建模)中每个层次对模型的影响和仅使用单个层次(SLL建模)对模型的影响。对于有效的局部建模策略,当使用多种工艺数据进行校准时,基于培养基或细胞生成的局部模型可以提供最佳结果,这种情况通常在工艺开发周期中发现。 此外,证明了基于不同克隆的本地模型在使用简化的过程数据集时具有很高的准确性。同时可以建立通用指南——例如,以标准操作程序 (SOP) 的形式,用于拉曼光谱 PAT 监测。一旦落实到位,这些指南还可以用于开发方案,以适应新的分子、工艺、产品模式,并为特定公司现有在使用 PAT(特别是拉曼光谱)的产品和平台技术创建更通用的方法。 参考文献: [1]Santos, Rafael M.Kaiser, PhilippMenezes, Jose C.Peinado, Antonio.Improving reliability of Raman spectroscopy for mAb production by upstream processes during bioprocess development stages[J].Talanta: The International Journal of Pure and Applied Analytical Chemistry, 2019, 199. | 产品分类
重点推荐产品
|
 |